“我本身是肝移植病人,没想到肝移植后还能以微创技术获得胃癌根治,更惊喜的是术后恢复如此之快。”近日,在复旦大学附属肿瘤医院黄华教授诊室内,75岁的姜先生来医院完成术后第一次随访。这位24年前曾因肝移植重获新生的“新肝宝贝”,通过仅5厘米的微创切口成功切除肿瘤,迎来了人生的“第三次生命”。
多学科联合攻坚难题,确定微创治疗方案
2001年,姜先生因突发肝硬化门脉高压肝功能衰竭并发上消化道出血,接受肝脏移植手术。2025年11月,姜先生陆续出现食欲减退、饭后腹胀、上腹痛等症状。起初他以为是小毛病,经胃镜检查,确诊为低分化腺癌,部分为印戒细胞癌,恶性程度较高。
由于姜先生有24年肝移植史,存在腹腔粘连、解剖结构变异等复杂情况,手术难度极大。此外,他口服抗排异药物最多只能停药两天,一旦停药时间过长,移植肝脏可能发生排异反应。他辗转多家医院,均被告知病情特殊手术风险过高而难以抉择。
今年11月下旬,姜先生慕名找到复旦大学附属肿瘤医院胃外1科黄华教授团队。了解患者复杂病史后,黄华第一时间召集胃外科、肝外科、麻醉科等多学科专家联合会诊,全面评估病情和根治手术的可能性。
“患者的核心需求是实现胃癌根治,同时尽快恢复胃肠功能,尽早恢复抗排异药物的服用。”黄华表示,综合评估后,微创手术在创伤小、恢复快方面的优势尤为关键,尽管预期腹腔粘连程度可能远超常规、抗排异药物停药‘窗口期’极短,团队仍决定迎难而上,尝试以微创方式完成高难度根治手术。
微创精细操作闯难关,犹如迷宫里拆炸弹
手术台上的挑战果然远超想象。腹腔镜镜头进入腹腔后,黄华团队发现,原本应自然垂下的网膜组织像“水帘洞”一样粘在前腹壁,术者就地取材巧妙运用吸引电凝棒和超声刀等能量设备钝锐结合分离找到组织间隙,再沿解剖层次逐步剥离,成功打开了手术通道。
随着手术的层层推进,发现胃与24年前移植的肝脏牢牢粘连,肝门部的胆管、肝动脉、门静脉因当年手术重构完全不可见,十二指肠与肝脏脏面也存在致密粘连,遍布的曲张血管稍一碰触就可能引发大出血,给手术视野暴露和操作带来极大阻碍。
“就像在迷宫里拆炸弹,每一步都要精准到毫米。”黄华带领团队制定了“先松解、再定位、后切除”的分步策略,全程在高清腹腔镜镜头的实时引导下精细操作。
“最关键的肝胃间隙粘连攻坚环节。”黄华说,他们整个团队操作过程更是慎之又慎。由于此处粘连组织内包裹着当年移植手术时重建的下腔静脉等多条重要血管,一旦损伤不仅会引发大出血,还可能影响移植肝脏的血供。
四个小时手术告捷,未出现任何并发症
外科团队采用超声刀结合电钩,以毫米级精度逐步松解粘连的大网膜和肠管,避免组织撕裂;同时结合术前胃镜定位标记和CT影像导航,精准锁定肿瘤位置,从胃后间隙作为突破口,逐步暴露肿瘤边界。
随后,团队改为前入路操作。黄华亲自操控器械,沿肝脏脏面、胃前壁及胃韧带致密粘连处缓慢游离,系统清扫胃周淋巴结,确保无肿瘤残留,最大程度降低复发和转移风险。在游离严重扭曲变形的十二指肠球部时,团队紧贴组织边缘精细操作,成功避开血管、胆管等重要结构。
最后,手术团队通过完全腹腔镜下胃肠吻合技术,完成消化道重建,吻合口采用可吸收缝线连续加强缝合,将术后吻合口漏等严重并发症的风险降至最低。经过四个小时奋战,手术成功。
与传统开腹手术相比,这台微创手术仅在腹壁留下一个约5厘米的辅助小切口用于取出标本,其余操作均通过腹腔镜小孔完成,切口明显更小。术后第二天,姜先生便可在病房内下床活动,肠道功能恢复排气并开始进食流质饮食,顺利自行服用抗排异药物,未出现任何并发症。
“没想到能挺过这一关,没想到开过‘大刀’还能做微创,没想到刀口这么小、恢复这么快。”姜先生用“三个没想到”总结自己的治疗经历。
据悉,复旦大学附属肿瘤医院是国内较早开展肿瘤微创诊疗的肿瘤专科医院,微创治疗已成为医院肿瘤外科治疗的核心特色之一。
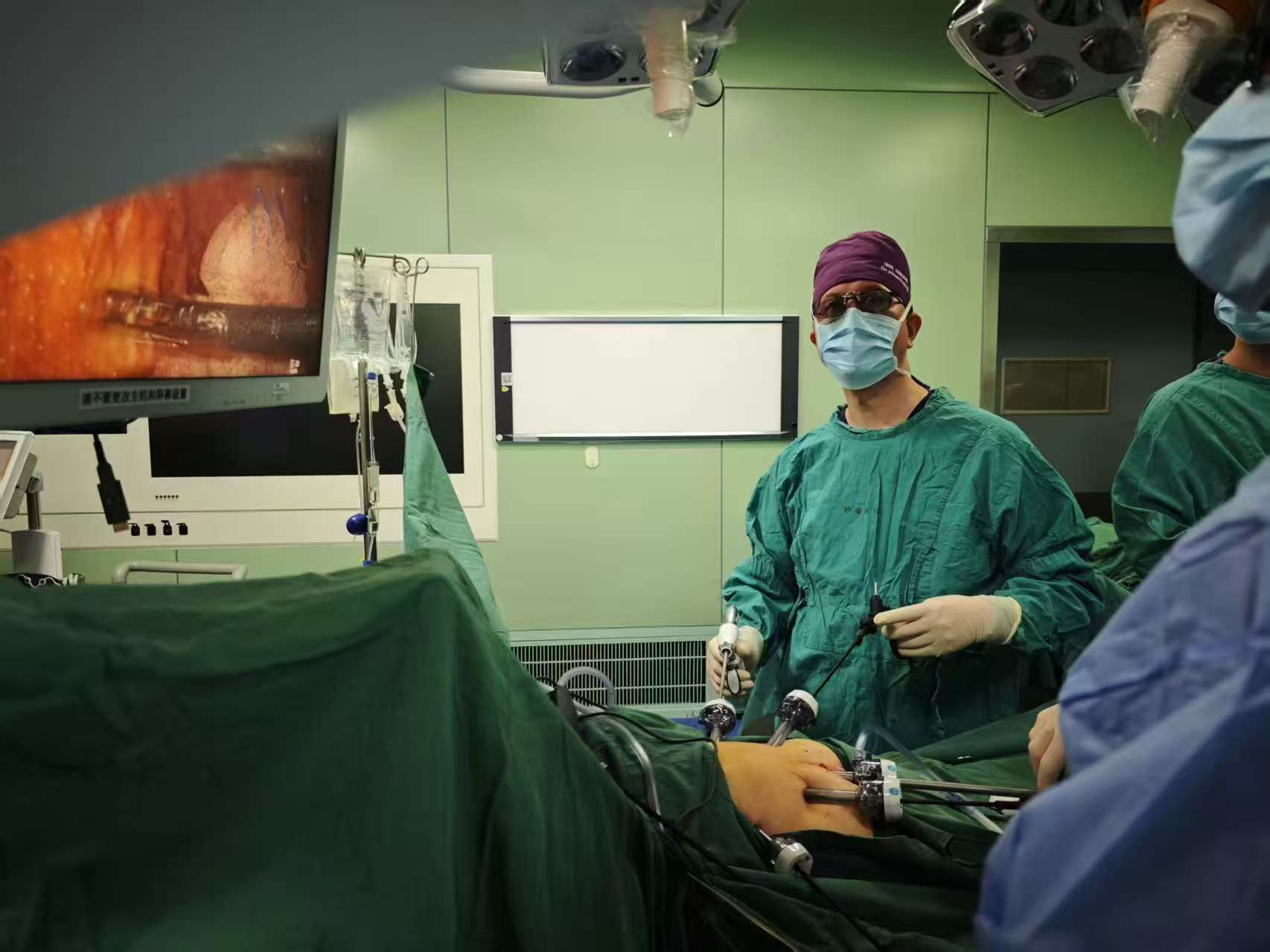
头图为手术过程中。受访者供图