日前,上海市胸科医院基础医学研究中心主任、检验科主任兼输血科主任王佳谊领衔,联合海内外多家研究团队,在国际顶级学术期刊《细胞》(Cell)发表最新研究成果。研究揭示了一种此前被忽视的肿瘤细胞死亡机制对免疫系统的影响,并提出了破解肿瘤免疫治疗困境的全新思路。
长期以来,学界普遍认为,治疗过程中肿瘤细胞被有效杀死,有助于激活机体免疫系统,从而进一步清除残余肿瘤细胞。然而,王佳谊团队通过系统比较多种细胞死亡方式后发现,并非所有“死亡”都会带来相同的免疫结果。有些细胞死亡方式能够“拉响警报”,显著激活免疫反应;而一种近年来备受关注的细胞死亡形式——“铁死亡”,虽然能够直接杀死肿瘤细胞,却并未有效唤醒免疫系统,甚至可能削弱免疫反应。
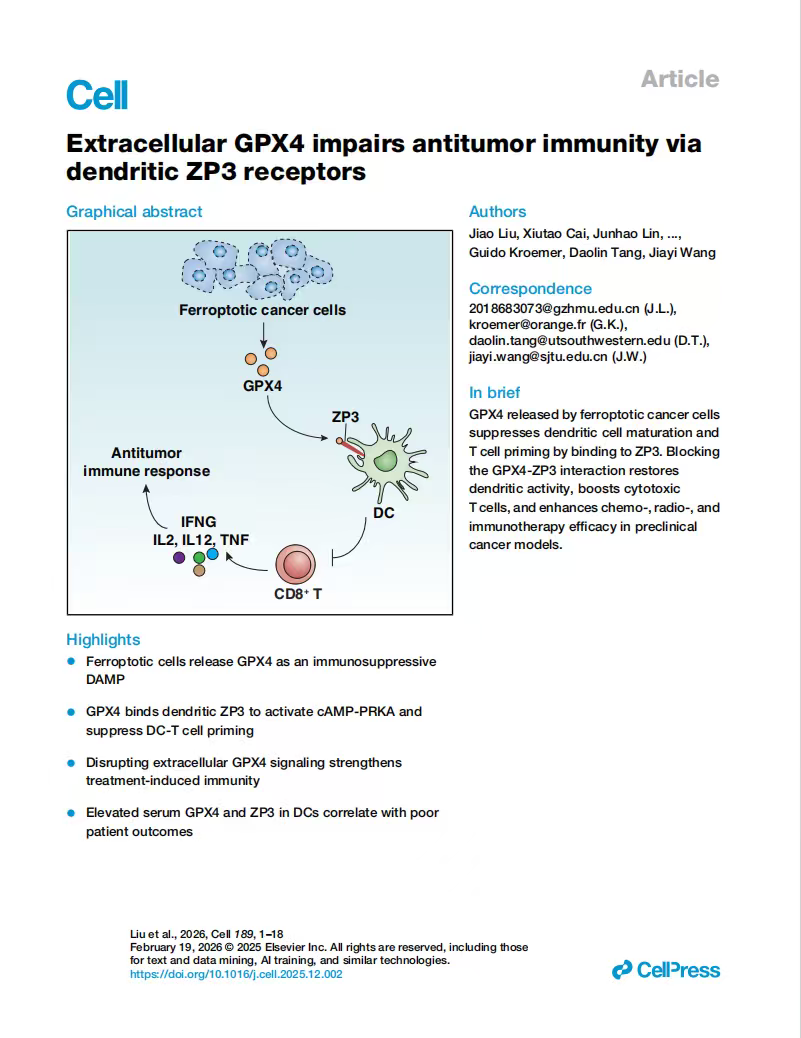
研究进一步发现,发生铁死亡的肿瘤细胞在死亡过程中会释放一种名为GPX4的蛋白。该蛋白并非单纯的细胞残留物,而是免疫系统中的“干扰项”,能够抑制免疫活性。机制研究显示,GPX4会与树突状细胞表面的ZP3受体结合,这一相互作用会导致整体抗肿瘤免疫反应明显减弱。
王佳谊团队发表在《cell》上论文的机制示意图。受访者供图
为验证这一机制的临床相关性,研究团队对大量患者临床样本及公共数据库进行了系统分析。结果显示,ZP3在胰腺癌、肺癌、肾癌等多种实体肿瘤中普遍呈现较高表达水平,且ZP3含量越高,患者预后往往越差。同时,在部分对化疗反应不佳的胰腺癌患者中,研究人员观察到其血液中GPX4水平明显升高。这些结果提示,GPX4和ZP3不仅在肿瘤免疫抑制过程中发挥重要作用,还有望成为评估免疫治疗疗效及患者预后的潜在生物标志物。
在多种小鼠肿瘤模型中,研究团队进一步尝试通过特异性抗体阻断GPX4与ZP3之间的相互作用。实验结果表明,这一干预手段能够显著逆转肿瘤微环境中的免疫抑制状态,使化疗、放疗及免疫治疗的抗肿瘤效果同步增强,并明显延长实验动物的生存时间。
研究团队指出,这一发现不仅为理解铁死亡在某些情况下削弱免疫治疗效果提供了重要解释,也为肿瘤免疫治疗的精准分型、疗效评估和联合治疗策略提供了新的靶点和方向。王佳谊表示,未来团队将继续推进相关临床转化研究,探索GPX4–ZP3这一新靶点在临床中的应用潜力,期待为更多患者带来更持久、更有效的免疫治疗获益。
头图为王佳谊团队正在进行研究。受访者供图